Thành phần để tạo nên thuốc thử cho việc chẩn đoán bệnh đầu vàng ở tôm sú giống bao gồm những loại nào? Cách thực hiện phản ứng Realtime RT PCR khi thực hiện phương pháp Realtime RT PCR ra sao?
Thành phần để tạo nên thuốc thử cho việc chẩn đoán bệnh đầu vàng ở tôm sú giống bao gồm những loại nào?
Theo Phụ lục A TCVN 8710-4:2019 về Bệnh thủy sản - Quy trình chẩn đoán - Phần 4: Bệnh đầu vàng ở tôm quy định về thành phần và việc chuẩn bị thuốc thử như sau:
"A.1 Dung dịch đệm TAE hoặc TBE
A.1.1 Thành phần
Dung dịch TAE (hoặc TBE) 10X: 100 ml
Nước khử ion: 900 ml
Tổng: 1000 ml dung dịch TAE (TBE) 1X
A.1.2 Chuẩn bị
Lấy 100 ml dung dịch TAE (TBE) 10X hòa chung với 900 ml nước khử ion, khuấy và lắc đều.
Bảo quản ở nhiệt độ phòng.
A.2 Dung dịch muối đệm phosphat (PBS)
A.2.1 Thành phần
Natri clorua (NaCl) 8 g
Natri hydro photphat dihydrat (Na2HPO4.2H2O) 2,9 g
Kali dihydro photphat (KH2PO4) 0,2 g
Kali clorua (KCl) 0,2 g
Nước cất 1000 ml
A.2.2 Chuẩn bị
Hòa tan các thành phần trên vào 1000ml nước cất, khuấy và lắc đều.
Chỉnh pH bằng dung dịch NaOH 1N hoặc dung dịch HCl 1N. Hấp vô trùng ở 121 °C trong 30 min."
Như vậy, thuốc thử cho việc chẩn đoán bệnh đầu vàng ở tôm sú giống bao gồm dung dịch đệm TAE hoặc TBE; dung dịch muối đệm phosphat (PBS) được tạo ra từ những thành phần được nêu trên.

Cách tiến hành phương pháp Realtime RT PCR để chẩn đoán bệnh đầu vàng ở tôm được quy định như thế nào?
Theo tiểu mục 6.2 Mục 6 TCVN 8710-4:2019 về Bệnh thủy sản - Quy trình chẩn đoán - Phần 4: Bệnh đầu vàng ở tôm quy định về việc chẩn đoán bệnh bệnh đầu vàng ở tôm bằng phương pháp Realtime RT PCR như sau:
"6 Chẩn đoán trong phòng thí nghiệm
...
6.2 Phương pháp Realtime RT - PCR
6.2.1 Lấy mẫu (Theo 6.1.1)
6.2.2 Bảo quản mẫu (Theo 6.1.2)
6.2.3 Chuẩn bị mẫu (Theo 6.1.3)
6.2.4 Cách tiến hành
6.2.4.1 Tách chiết ARN
Sử dụng bộ kít tách chiết (3.2.3) thích hợp và an toàn theo hướng dẫn của nhà sản xuất.
VÍ DỤ: Sử dụng kit tách chiết ARN: PureLinK Viral RNA/DNAMini kit (50) (Lot 1361246)[2]) (xem phụ lục B)
6.2.4.2 Chuẩn bị mồi
Phương pháp Realtime RT-PCR sử dụng cặp mồi YHV 141F / YHV 206R và YHV p (3.2.2) để phát hiện vi rút đầu vàng YHV1. Trình tự cặp mồi (xem phụ lục D, Bảng D.1).
Mồi ở trạng thái đông khô phải được ly tâm nhanh bằng máy spindown (4.1.5) trong 30 s để mồi lắng xuống đáy ống trước khi mở và hoàn nguyên. Dùng dung dịch đệm TE (3.2.6) để hoàn nguyên mồi ở nồng độ 100 µM làm gốc.
Mồi được sử dụng ở nồng độ 20 µM: Pha loãng mồi gốc bằng nước tinh khiết không có nuclease (3.2.8) (10 µl mồi gốc và 40 µl nước tinh khiết không có nuclease).
Đoạn dò YHV-p sử dụng nồng độ 6 µM: Pha loãng đoạn dò bằng nước tinh khiết không có nuclease (3.2.8) (3 µl mồi gốc và 47 µl nước tinh khiết không có nuclease).
6.2.4.3 Thực hiện phản ứng Realtime RT-PCR
Phản ứng khuếch đại được thực hiện trong máy Realtime PCR (4.1.2) theo phương pháp Realtime RT- PCR khuếch đại đoạn gen đặc hiệu của vi rút đầu vàng YHV1 sử dụng cặp mồi YHV 141F / YHV 206R và YHV p (3.2.2) (xem phụ lục D).
6.2.4.4. Đọc kết quả
Điều kiện phản ứng được công nhận khi:
- Mẫu đối chứng âm phải cho kết quả âm tính (không có giá trị Ct);
- Mẫu đối chứng dương phải cho kết quả dương tính và có giá trị Ct so với giá trị Ct của mẫu đã được chuẩn độ trước đó có khoảng giá trị Ct dao động ± 2.
Với điều kiện phản ứng như trên:
- Mẫu có giá trị Ct < 35 được xem là dương tính;
- Mẫu không có giá trị Ct là âm tính;
- Mẫu có giá trị Ct trong khoảng 35 ≤ Ct ≤ 40 được xem là nghi ngờ.
CHÚ Ý: - Những mẫu nghi ngờ, cần được thực hiện lại xét nghiệm hoặc sử dụng phương pháp xét nghiệm tương đương khác để khẳng định kết quả;
- Phản ứng realtime RT-PCR phải bao gồm: mẫu kiểm tra, mẫu đối chứng dương và mẫu đối chứng âm;
- Mẫu và nguyên liệu cho phản ứng realtime RT-PCR cần đặt trong khay đá lạnh trong suốt quá trình chuẩn bị hỗn hợp phản ứng.
...."
Theo đó, trình tự tiến hành phương pháp Realtime RT PCR phải tuân theo trình tự được quy định tại tiểu mục 6.2.4 Mục 6 TCVN 8710-4:2019 vừa nêu trên.
Cách thực hiện phản ứng Realtime RT PCR khi thực hiện phương pháp Realtime RT PCR ra sao?
Theo Phục lục D TCVN 8710-4:2019 về Bệnh thủy sản - Quy trình chẩn đoán - Phần 4: Bệnh đầu vàng ở tôm quy định về phản ứng Realtime RT PCR như sau:
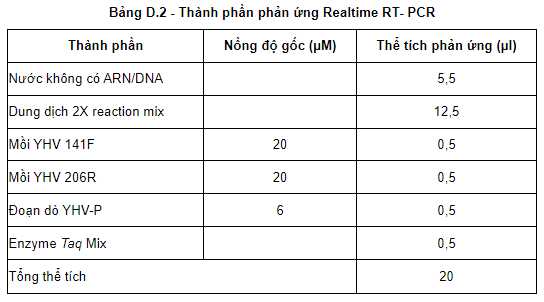
"D.2 Thực hiện phản ứng Realtime RT- PCR
Phương pháp Realtime RT-PCR khuếch đại đoạn gen đặc hiệu của YHV1, sử dụng cặp mồi đã được chuẩn bị (3.2.2) và kít nhân gen (3.2.5) theo hướng dẫn của nhà sản xuất.
VÍ DỤ: theo kít SuperScript III Platinum® one step qRT-PCR System, Cat.No: 11732-020[4])
Thành phần cho 1 phản ứng (xem Bảng D.2).
Chuyển 20 µl hỗn hợp nhân gen vào mỗi ống phản ứng:
- Mẫu đối chứng dương: Cho 5 µl mẫu ARN được tách chiết từ mẫu dương tính chuẩn với YHV1;
- Mẫu đối chứng âm: Cho 5 µl nước tinh khiết không có nuclease;
- Mẫu thử: Cho 5 pl mẫu ARN kiểm tra vào ống phản ứng.
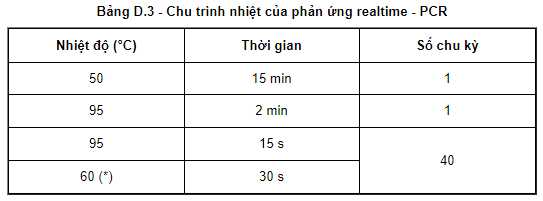
Tiến hành phản ứng realtime PCR bằng máy nhân gen (4.1.2) đã cài đặt chu trình nhiệt (xem Bảng D.3)."
Như vậy, khi thực hiện phản ứng Realtime RT PCR sẽ có hai phản ứng xảy ra là thành phần phản ứng và chu trình nhiệt phản ứng.
Căn cứ vào số liệu quy định tại 2 bảng nêu trên trại Phục lục D TCVN 8710-4:2019 mà tiến hành phản ứng Realtime RT PCR.










Quý khách cần hỏi thêm thông tin về có thể đặt câu hỏi tại đây.
- Mẫu đơn đề nghị sáp nhập hội mới nhất? Hướng dẫn làm đơn đề nghị sáp nhập hội như thế nào?
- Thủ tục gia hạn hoặc điều chỉnh hoạt động liên kết đào tạo trình độ đại học, thạc sĩ, tiến sĩ tại Quyết định 3278 như thế nào?
- Thủ tục đề xuất cơ chế ưu đãi đầu tư theo Quyết định 891 của Bộ Xây dựng thực hiện ở cấp tỉnh như thế nào?
- Các cơ quan lãnh đạo hội do Đảng, Nhà nước giao nhiệm vụ theo Nghị định 126 được quy định như thế nào?
- Thủ tục cấp Giấy chứng nhận đăng ký kết nối để cung cấp dịch vụ nội dung thông tin trên mạng viễn thông di động ra sao?