TIÊU
CHUẨN QUỐC GIA
TCVN
11319:2016
ISO
14852:1999
XÁC ĐỊNH KHẢ NĂNG PHÂN HỦY SINH HỌC HIẾU KHÍ HOÀN TOÀN CỦA
CÁC VẬT LIỆU NHỰA TRONG MÔI TRƯỜNG NƯỚC - PHÂN TÍCH LƯỢNG CACBON DIOXIT PHÁT
SINH
Determination
of the ultimate aerobic biodegradability of plastic materials in an aqueous medium
- Method by analysis of evolved carbon dioxide
Lời nói đầu
TCVN 11319:2016 hoàn toàn tương đương với ISO
14852:1999 và đính chính kỹ thuật 1:2005
TCVN 11319:2016 do Tổng cục Môi trường biên
soạn, Bộ Tài nguyên và Môi trường đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng
thẩm định, Bộ Khoa học và Công nghệ công bố.
Lời giới thiệu
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
XÁC ĐỊNH KHẢ NĂNG
PHÂN HỦY SINH HỌC HIẾU KHÍ HOÀN TOÀN CỦA CÁC VẬT LIỆU NHỰA TRONG MÔI TRƯỜNG NƯỚC
- PHÂN TÍCH LƯỢNG CACBON DIOXIT PHÁT SINH
Determination
of the ultimate aerobic biodegradability of plastic materials in an aqueous
medium - Method by analysis of evolved carbon dioxide
CẢNH BÁO Trong nước thải,
bùn hoạt tính, đất và
compost có thể tồn tại các sinh vật gây bệnh, do đó cần có
biện pháp đề phòng thích hợp khi xử lý các chất này. Nên cẩn thận với
các chất thử có độc tính
và các chất chưa biết rõ tính chất.
1 Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp
xác định mức độ phân hủy sinh học hiếu khí của vật liệu chất dẻo, bao gồm cả các
vật liệu có chứa các phụ gia, bằng cách đo lượng cacbon dioxit sinh ra. Vật
liệu thử được cho tiếp xúc trong một môi trường tổng hợp dưới các điều kiện thử nghiệm với
vật liệu cấy được lấy từ bùn hoạt hóa, compost hoặc đất.
Nếu sử dụng bùn hoạt hóa
không thích ứng làm vật liệu cấy thì phép thử này mô phỏng quá trình
phân hủy sinh học xảy ra trong môi trường nước tự nhiên; nếu sử dụng vật liệu cấy đã được cho tiếp
xúc trước hoặc trộn sẵn thì có thể sử dụng phương pháp này để kiểm tra khả năng phân hủy
sinh học tiềm ẩn của vật liệu
thử.
Các điều kiện được sử dụng trong tiêu
chuẩn này không cần
thiết phải giống với các điều kiện tối ưu để quá trình phân hủy sinh học tối đa xảy ra,
nhưng tiêu chuẩn này được xây dựng để xác định khả năng phân hủy sinh học tiềm ẩn của các
vật liệu chất dẻo hoặc đưa ra
chỉ dẫn về khả năng phân hủy sinh học của vật liệu trong các môi trường tự
nhiên.
Phương pháp này giúp cho việc đánh giá khả năng
phân hủy sinh học có
thể được cải thiện bằng
cách tính toán cân bằng cacbon (tùy chọn, xem phụ lục C).
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
- Polyme tổng hợp và/hoặc tự nhiên, polyme đồng
trùng hợp (copolyme) hoặc hỗn hợp của cả hai;
- Vật liệu chất dẻo có các phụ gia
như chất hóa dẻo, chất
màu hoặc các hợp chất khác;
- Polyme tan được trong nước;
- Vật liệu mà trong các điều kiện của phép thử
không ức chế các vi
sinh
vật có trong vật liệu cấy. Có thể xác định các ảnh hưởng ức chế bằng cách sử dụng
phương án kiểm soát ức chế hoặc một phương pháp thích hợp khác (ví dụ xem ISO
8192[3]). Nếu vật liệu thử ức chế vi sinh
vật trong vật liệu cấy thì sử dụng loại vật liệu cấy khác hoặc sử dụng
vật liệu cấy được phơi nhiễm trước với nồng độ thử thấp hơn.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho
việc áp dụng tiêu chuẩn này. Đối với các tài liệu
viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu
viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm
cả các sửa đổi, bổ sung (nếu có).
TCVN 6834:2000 (ISO 8245:1999), Chất
lượng nước -
Hướng
dẫn xác định cacbon hữu cơ tổng số (TOC)
và cacbon hữu cơ hòa tan (DOC).
TCVN 6489:2009 (ISO 9439:1999), Chất
lượng nước - Đánh giá khả năng phân hủy sinh học hiếu khí hoàn toàn của
các hợp chất hữu cơ
trong môi trường nước - Phép thử sự giải phóng cacbon dioxit.
TCVN 6981:2001 (ISO 10634:1995), Chất
lượng nước - Hướng dẫn chuẩn bị và xử lý hợp chất hữu cơ
ít tan trong nước để đánh giá sự phân hủy sinh học trong môi trường nước.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
3 Thuật ngữ và định
nghĩa
Trong tiêu chuẩn này, áp dụng các thuật
ngữ và định nghĩa sau đây
3.1
Phân hủy sinh học hiếu khí hoàn toàn (ultimate
aerobic biodegradation)
Phân hủy một hợp chất hữu cơ
bởi các vi sinh
vật khi có mặt oxy, tạo
thành cacbon dioxit, nước và
muối khoáng của nguyên tố bất kỳ có mặt (quá trình khoáng hóa) cộng
với sinh khối mới.
3.2
Bùn hoạt hóa (activated sludge)
Sinh khối tạo thành trong quá trình xử lý
hiếu khí nước thải do sự phát
triển của vi khuẩn và các vi
sinh vật khác khi có mặt của oxy hòa tan.
3.3
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Lượng chất rắn thu được bằng cách lọc
hoặc ly tâm một thể tích bùn hoạt hóa biết trước và sấy khô ở khoảng 105
°C đến khối lượng
không đổi.
3.4
Cacbon vô cơ hòa tan (dissolved
inorganic carbon)
DIC
Phần cacbon vô cơ trong nước mà không
thể loại bỏ được bằng quá trình phân tách
pha quy định, ví dụ bằng
cách ly tâm trong 15 min ở 40 000 m.s-2 hoặc bằng
cách lọc qua màng lọc có đường
kính lỗ từ 0,2 μm đến
0,45
μm.
3.5
Lượng cacbon dioxit sinh ra
theo lý thuyết (theoretical amount of evolved carbon dioxide)
ThCO2
Lượng cacbon dioxit tối đa theo lý
thuyết được sinh ra sau khi oxy hóa hoàn toàn một hợp chất hóa học, được tính từ
công thức phân tử, biểu thị bằng mlligam cacbon dioxit sinh ra trên
miligam hoặc gam hợp chất thử.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Tổng số cacbon hữu cơ (total
organic carbon)
TOC
Tất cả cacbon có trong một hợp
chất hữu cơ, hòa tan hoặc lơ
lửng trong nước.
3.7
Cacbon hữu cơ hòa tan (dissolved
organic carbon)
DOC
Phần cacbon hữu cơ trong nước
mà không thể loại bỏ được bằng quá trình phân tách pha quy định, ví dụ bằng cách ly
tâm trong 15 min ở 40.000 m.s-2 hoặc bằng
cách lọc qua màng lọc có đường kính lỗ
từ 0,2 μm đến 0,45 μm.
3.8
Giai đoạn thích ứng (lag phase)
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
3.9
Mức độ phân hủy sinh học tối đa (maximum
level of biodegradation)
Mức độ phân hủy sinh học, tính bằng phần trăm,
của một hợp chất hóa học hoặc chất hữu cơ trong một phép thử mà trên mức đó sự
phân hủy sinh học không còn xảy ra thêm nữa.
3.10
Giai đoạn phân hủy sinh học
(biodegradation phase)
Thời gian, tính bằng ngày, từ khi kết
thúc giai đoạn thích ứng của phép
thử cho đến khi
đạt được khoảng 90 % mức phân hủy sinh học tối đa.
3.11
Giai đoạn ổn định (plateau
phase)
Thời gian, tính bằng ngày, từ
khi kết thúc giai đoạn phân hủy sinh học cho đến khi kết thúc phép thử.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Tiếp xúc trước
(pre-exposure)
Quá trình tiếp xúc trước vật liệu
cấy với hợp chất hóa học hoặc chất
hữu cơ cần thử để tăng khả năng của vật liệu cấy phân hủy sinh học vật liệu thử
bằng cách làm thích nghi và/hoặc chọn lọc các vi sinh vật.
3.13
Làm thích nghi trước
(pre-conditioning)
Quá trình tiếp xúc trước vật liệu cấy
trong các điều kiện của phép thử sau đỏ nhưng không có mặt của hợp chất hóa học
hoặc chất hữu cơ cần thử để cải thiện tính năng của phép thử bằng cách cho vi
sinh vật thích nghi với các điều kiện của phép thử.
4 Nguyên tắc
Khả năng phân hủy sinh học của một vật
liệu chất
dẻo
được xác định bằng cách
sử dụng các vi sinh vật hiếu khí trong môi trường nước. Hỗn hợp thử gồm môi trường vô cơ,
vật liệu thử hữu cơ (nguồn cacbon và năng lượng duy nhất) có nồng độ cacbon hữu
cơ từ 100 mg/I đến 2000 mg/l và vật liệu cấy là bùn hoạt hóa hoặc huyền phù của
đất hoạt tính hoặc compost. Hỗn hợp này được khuấy trộn trong các bình thử và được làm
thoáng khí bằng không khí không có
cacbon dioxit trong một khoảng thời gian tùy thuộc vào động học của quá trình
phân hủy sinh học, nhưng không được quá 6 tháng. Lượng cacbon dioxit sinh ra
trong quá trình phân hủy sinh học được xác định bằng phương pháp phân tích phù hợp,
như các ví dụ trong Phụ
lục A và B.
Mức phân hủy sinh học, biểu thị bằng
phần trăm, được xác định bằng cách so sánh lượng cacbon dioxit sinh ra với lượng cacbon
dioxit sinh ra
theo lý thuyết (ThCO2). Kết quả thử
là mức phân hủy sinh học tối đa
được xác định từ giai đoạn ổn định của đồ thị phân hủy sinh học. Ngoài ra, có
thể tính toán cân bằng cacbon để cung cấp thông tin bổ sung cho quá trình phân hủy sinh học
(xem phụ lục C).
Khác với TCVN 6489 (ISO 9439), sử dụng
được cho các hợp chất hữu cơ khác nhau, tiêu chuẩn này được sử dụng để xác định
khả năng phân hủy sinh học của các vật liệu chất dẻo. Các yêu cầu đặc biệt
này tác động đến việc lựa chọn vật liệu cấy và môi trường thử và có khả
năng cải thiện sự đánh giá khả năng phân hủy sinh học thông qua việc tính cân bằng
cacbon.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Quá trình ủ phải được thực hiện trong
bóng tối hoặc
trong ánh sáng khuếch tán, trong một không gian khép kín không
chứa các hơi có thể ức chế vi sinh vật và được duy trì ở nhiệt độ không đổi, tốt nhất từ 20 °C đến 25 °C, dao động
trong khoảng ± 1 °C hoặc tại nhiệt
độ thích hợp khác phụ thuộc vào vật liệu cấy sử dụng và môi trường cần đánh
giá.
CHÚ THÍCH Đối với vật liệu cấy
compost, sử dụng nhiệt độ cao hơn có thể phù hợp.
6 Thuốc thử
Chỉ sử dụng thuốc thử loại tinh khiết phân tích.
6.1 Nước cất hoặc
nước khử ion, không có độc tố (đặc
biệt là đồng) và có hàm lượng
DOC nhỏ hơn 2 mg/I.
6.2 Môi trường thử
Tùy thuộc vào mục đích của phép thử,
có thể sử dụng môi trường thử khác nhau. Ví dụ, nếu mô phỏng một môi trường tự
nhiên thì sử dụng môi
trường thử chuẩn (6.2.1). Nếu vật liệu thử được sử dụng ở nồng độ cao hơn thì sử
dụng môi trường thử tối ưu
(6.2.2) với lượng đệm và nồng độ chất dinh dưỡng cao hơn.
6.2.1 Môi trường thử chuẩn
6.2.1.1 Dung dịch A
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Kali dihydro photphat khan (KH2PO4)
8,5 g
Dikali hydro phophat khan (K2HPO) 21,75 g
Dinatri hydro photphat dihydrat (Na2HPO4.2H2O) 33,4 g
Amoni clorua (NH4CI) 0,5 g
trong nước (6,1) và cho thêm nước đến
1 000 ml.
CHÚ THÍCH Có thể kiểm tra thành
phần chính xác của dung dịch bằng cách đo pH, giá trị phải bằng
7,4.
6.2.1.2 Dung dịch B
Hòa tan 22,5 g magie sunphat
heptahydrat (MgSO4.7H2O) trong nước
(6.1) và thêm nước đến 1 000 ml.
6.2.1.3 Dung dịch C
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
6.2.1.4 Dung dịch D
Hòa tan 0,25 g sắt (III) clorua
hexahydrat (FeCl3.6H2O) trong nước (6.1) và thêm nước đến 1 000 ml.
Chuẩn bị dung dịch này ngay trước khi sử dụng để tránh kết tủa,
hoặc thêm một giọt axit clohydric đậm đặc (HCl) hoặc một giọt dung dịch nước của etylendiamintetraaxetic
axit 0,4 g/l (EDTA).
6.2.1.5 Chuẩn bị
Để chuẩn bị 1 lít môi trường thử thì
thêm vào khoảng 500
ml nước (6.1)
- 10 ml dung dịch A;
- 1 ml mỗi dung dịch từ B đến D.
Cho thêm nước
(6.1) đến 1000 ml.
6.2.2 Môi trường thử tối ưu
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
6.2.2.1 Dung dịch A
Hòa tan
Kali dihydro photphat khan (KH2PO4) 37,5 g
Dinatri hydro photphat dihydrat (Na2HPO4.2H2O)
87,3 g
Amoni clorua (NH4Cl) 2,0 g
trong nước (6.1) và cho thêm nước đến
1 000 ml.
6.2.2.2 Dung dịch B
Hòa tan 22,5 g magie sunphat
heptahydrat (MgSO4.7H2O) trong nước
(6.1) và thêm nước đến 1 000 ml.
6.2.2.3 Dung dịch C
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
6.2.2.4 Dung dịch D
Hòa tan 0,25 g sắt (III) clorua
hexahydrat (FeCl3.6H2O) trong nước (6.1) và thêm nước đến 1 000 ml.
6.2.2.5 Dung dịch E (dung dịch vết nguyên tố,
tùy chọn)
Hòa tan trong 10 ml dung dịch nước HCl
(25 %, 7,7 mol/l) theo thứ tự sau:
10 mg ZnCl2 100 mg MnCl2.4H2O, 6 mg H3BO3, 190 mg CoCI2.6H2O, 3 mg CuCI2.2H2O, 240 mg NiCI2.6H2O, 36 mg Na2MoO4.2H2O, 33 mg Na2WO4.2H2O và 26 mg Na2SeO3.5H2O và cho thêm nước
đến 1000 ml (6.1).
6.2.2.6 Dung dịch F (dung dịch vitamin,
tùy chọn)
Hòa tan vào 100 ml nước (6.1) 0,6 mg
biotin, 2,0 mg niacinamin,
2,0 mg p-aminobenzoate, 1,0 mg axit pantotenic, 10,0 mg pyridoxal
hydrocloma, 5,0 mg cyanocobalamlne, 2,0 mg axit folic, 5,0 mg riboflavin, 5,0
mg DL-thioctic axit và 1,0 mg thiamine dichloride hoặc sử dụng dung dịch 15 mg chất
chiết men trong 100 ml nước (6.1). Lọc dung dịch này qua thiết bị
lọc màng để khử trùng (xem 7.6).
CHÚ THÍCH Dung dịch E và F là
tùy chọn và không yêu cầu
nếu sử dụng nồng độ vật liệu cấy vừa đủ, ví dụ như bùn hoạt hóa, đất hoặc
compost. Nên chuẩn bị các phần
1 ml một và bảo quản lạnh
cho đến khi
sử
dụng.
6.2.2.7 Chuẩn bị
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
- 100 ml dung dịch A;
- 1 ml từng dung dịch từ B đến D và, tùy chọn E và F.
Cho thêm nước (6.1) đến 1000 ml và đo
pH.
CHÚ THÍCH Có thể kiểm tra thành phần chính xác của
dung dịch bằng cách đo pH, giá trị phải bằng 7,0 ± 0,2.
6.3 Dung dỊch
pyrophotphat
Hòa tan 2,66 g natri pyrophotphat khan
(Na4P2O7) trong nước
(6.1) và cho thêm nước
đến 1 000 ml
6.4 Chất hấp thụ
cacbon dioxit, các hạt xút
hoặc chất hấp thụ khác thích hợp.
7 Thiết bị, dụng cụ
Tất cả các thiết bị thử phải sạch và đặc
biệt không có vật liệu vô
cơ và độc tố.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
7.1 Bình thử nghiệm, gồm các bình thủy tinh (như bình
tam giác hoặc chai) được thiết kế để có thể đuổi sạch khí và khuấy hoặc lắc, có lắp ống không
thấm khí CO2. Các bình phải được đặt
trong một phòng có
nhiệt
độ không đổi hoặc trong một thiết bị, dụng cụ ổn nhiệt (như bể cách thủy).
7.2 Hệ thống cấp
khí không chứa CO2, có khả năng
cung cấp vào từng bình thử nghiệm
không khí không chứa
cacbon dioxit ở tốc độ dòng
trong khoảng từ 50 ml/min đến 100 ml/min, được giữ ổn định với độ chính xác
± 10 % (xem ví dụ về hệ thống gồm cả các bình thử trong Phụ lục A).
7.3 Thiết bị phân tích
dùng để xác định cacbon dioxit, bao gồm các
thiết bị thích hợp có đủ độ chính
xác, ví dụ thiết bị
phân tích CO2 hoặc DIC hoặc
thiết bị xác định việc
chuẩn độ sau khi
hấp thụ hoàn toàn trong một dung dịch kiềm (xem ví dụ trong Phụ lục B). Lưu ý rằng nếu sử
dụng thiết bị phân tích có
detector IR thì không cần sử
dụng khí không chứa CO2.
7.4 Thiết bị phân
tích dùng để xác định cacbon hữu cơ tổng số (TOC) và cacbon hữu cơ hòa tan (DOC) [xem TCVN
6634 (ISO 8245)].
7.5 Cân phân tích (loại sử dụng
trong phòng thí
nghiệm)
7.6 Thiết bị ly
tâm
hoặc thiết bị lọc có tấm màng lọc
(cỡ lỗ 0,45 μm) không hấp phụ hoặc giải phóng cacbon hữu cơ.
7.7 Thiết bị đo
pH
(loại sử dụng trong phòng thí nghiệm)
7.8 Máy khuấy từ
hoặc máy lắc
(loại sử dụng trong phòng thí nghiệm)
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
8.1 Vật liệu thử
Vật liệu thử phải là vật liệu có khối
lượng đã biết và chứa lượng cacbon đủ tạo một lượng CO2 mà có thể được
xác định chính xác bằng hệ
thống phân tích sử dụng. Tính TOC theo công thức hóa học hoặc xác định bằng kỹ
thuật phân tích phù hợp
[ví dụ phân tích nguyên tố hoặc xác định
theo TCVN 6634 (ISO 8245)] và tính lượng ThCO2. Sử dụng nồng độ vật
liệu thử sao cho hàm lượng TOC ít nhất bằng 100 mg/l. Lượng vật liệu thử tối đa bị giới hạn
bởi lượng oxy
cung cấp cho hệ thống thử và môi trường thử được sử dụng. Khi sử dụng môi trường thử tối ưu (6.2.2),
nồng độ của vật liệu thử phải ở mức sao cho lượng TOC không vượt quá 2 000 mg/l, nghĩa
là tỷ lệ C:N khoảng 40:1. Nếu sử dụng nồng độ cao hơn thì phải tăng lượng
nitơ trong môi trường thử.
CHÚ THÍCH Nên ưu tiên
sử dụng vật liệu
thử ở dạng bột nhưng cũng có thể sử dụng vật liệu dạng màng, mảnh nhỏ hay
các hạt định hình; Kích thước
và hình dạng của vật
liệu thử có
thể
ảnh hưởng đến khả
năng phân hủy sinh học của chúng. Nếu để so sánh các loại vật liệu chất dẻo khác
nhau thì nên sử dụng các vật liệu có hình dạng tương tự nhau. Nếu vật liệu thử có dạng
bột thì phải sử dụng
các hạt nhỏ đã biết trước sự phân bố kích thước và nên sử dụng phân bố kích thước hạt
với đường kính tối đa là 250 μm.
Tương tự như vậy, kích thước của
thiết bị sử dụng cũng phụ thuộc vào thể loại vật liệu thử. Phải đảm bảo chắc chắn rằng
không có các thay đổi
cơ học không mong muốn xảy ra do các điều kiện của phép thử, ví dụ như là cơ
cấu khuấy. Việc gia công, chế biến vật liệu thử không có ảnh hưởng
đáng kể đến sự phân
hủy của vật liệu (ví
dụ
trong trường hợp sử dụng vật liệu dạng bột đối với các hỗn hợp). Có thể xác định
hàm lượng hydro, oxy, nitơ, photpho
và lưu huỳnh cũng như khối lượng phân tử của vật liệu thử bằng phương pháp sắc
ký thẩm thấu gel (ví dụ xem ASTM D
3536-91[1]) hoặc tiêu
chuẩn khác thích
hợp. Ưu tiên thử nghiệm vật
liệu chất dẻo không có phụ gia như
chất hóa dẻo. Khi vật liệu chứa các chất phụ gia như vậy thì cần phải có thông
tin về khả năng phân hủy
sinh học của các chất phụ gia để có thể đánh giá được khả năng phân hủy sinh học của
chính vật liệu polyme đó.
Để biết thêm thông tin chi tiết về cách xử lý đối
với các hợp chất ít tan trong nước,
xem TCVN 6918 (ISO 10634).
8.2 Vật liệu đối
chứng
Sử dụng anilin và/hoặc polyme có khả
năng phân hủy sinh học tốt làm vật liệu đối chứng [ví dụ bột cellulose vì tinh thể, giấy
lọc xenlulo không tàn hoặc poly (β-hydroxybutyrat)]. Nếu có thể, thể loại và
kích thước, lượng
TOC của vật liệu đối chứng phải có khả năng so sánh được với hình dạng, kích
thước và lượng TOC của vật liệu thử.
Có thể sử dụng polyme không phân hủy sinh học
(ví dụ polyetylen) có cùng hình dạng với vật liệu thử làm vật liệu
đối chứng âm.
8.3 Chuẩn bị vật liệu cấy
Bùn hoạt hóa từ các trạm
xử lý nước thải xử lý chủ yếu nước thải sinh hoạt là nguồn phù hợp để cung cấp vật liệu cấy. Bùn
này được lấy từ môi trường hiếu khí hoạt động và có sẵn ở khắp một
vùng diện tích địa lý rộng
lớn, trong đó nhiều loại vật
liệu chất dẻo cần được thử nghiệm. Ngoài ra, có thể sử dụng đất và/hoặc huyền
phù compost cho quá trình cấy vì với một số loại vật liệu chất dẻo thì hoạt động của
nấm đóng vai
trò quan trọng đối với quá trình phân hủy sinh học. Khi xác định được quá trình
phân hủy sinh học trong một hệ thống xử lý chất thải cụ thể thì lấy vật liệu cấy từ môi trường đó.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
CHÚ THÍCH Việc xác định đơn vị cụm khuẩn (cfu) của vật
liệu cấy sử dụng có thể
sẽ hữu ích. Hỗn hợp
thử nên chứa khoảng từ 103 đến 106 cfu/ml.
8.3.1 Vật liệu cấy lấy
từ trạm xử lý nước thải
Lấy một mẫu bùn hoạt hóa được thu thập
từ trạm xử lý nước thải đã được vận hành hoặc khu thí nghiệm xử lý nước thải sinh hoạt. Trộn
đều và giữ mẫu dưới các điều kiện hiếu khí và tốt nhất là sử dụng ngay trong
ngày (tối thiểu trong 72 h).
Trước khi sử dụng, xác định nồng độ của
các chất rắn lơ lửng (ví dụ
theo ISO 11923
[3]). Nếu cần thiết, cô đặc
bùn này bằng cách để lắng sao cho thể tích của bùn được thêm vào cho phép thử là nhỏ nhất. Thêm một
lượng phù hợp để thu được hàm lượng chất rắn lơ lửng trong hỗn hợp cuối từ 30 mg/l đến 1000 mg/l.
CHÚ THÍCH 1 Khi quá trình phân hủy sinh học trong môi trường tự nhiên
được mô phỏng hoặc khi
tiến hành xác định cân bằng cacbon (xem Phụ lục C) thì nên sử dụng vật liệu cấy
có hàm lượng chất rắn lơ lửng là 30 mg/l. Vì các chất rắn có thể cản trở việc xác định
cân bằng cacbon nên phải tuân theo quy trình chuẩn bị vật liệu cấy như sau. Lấy
500 ml
bùn
hoạt hóa và làm đồng nhất
trong 2 min với
tốc độ trung bình trong một
bình trộn hoặc máy trộn phù hợp
tốc độ cao. Để hỗn hợp lắng cho đến khi chất lỏng nổi phía trên chứa một lượng không đáng kể các chất lơ lửng nhưng không được lâu
hơn 30 min. Gạn lượng chất lỏng nổi phía trên và cho vào bình thử để có được nồng
độ là 1 % (V/V) đến 5 % (V/V) trong môi
trường thử. Tránh gạn cả các hạt bùn.
CHÚ THÍCH 2 Vật liệu cấy để có thể được
làm thích nghi trước nhưng
không sử dụng vật liệu cấy đã được cho
tiếp xúc trước, nhất là trong trường
hợp phép thử mô phỏng đặc tính phân hủy sinh học trong môi trường tự
nhiên. Tùy vào mục đích của phép
thử có thể sử dụng
vật liệu cấy được tiếp xúc trước miễn
là trong báo cáo thử nghiệm phải nêu rõ điều này (ví dụ phần trăm phân hủy sinh
học = x %, sử dụng vật liệu cấy được tiếp xúc trước)
và phương pháp tiếp xúc trước
cũng phải được nêu chi tiết
trong báo cáo thử nghiệm. Vật
liệu cấy được tiếp
xúc trước có thể lấy từ các phép
thử phân hủy
sinh học trong phòng thí nghiệm phù hợp
(xem ISO/TR 15462) được thực hiện trong các điều kiện khác nhau hoặc từ các mẫu
thử được lấy từ
các địa điểm mà ở đó có các điều kiện
môi trường tương
đương (ví dụ khu vực bị ô nhiễm hoặc trạm xử lý chất thải công nghiệp).
8.3.2 Vật liệu cấy
lấy từ đất và/hoặc compost
Hòa 10 g đất màu mỡ hoặc compost lấy từ bãi
compost xử lý chất thải, hữu cơ
trong 100 ml môi trường thử (6.2.1 hoặc 6 2.2) hoặc trong dung dịch pyrophotphat
(6.3) mà thường được sử dụng trong lĩnh vực vi sinh vật đất. Để lắng dung
dịch trong khoảng 30 min. Gạn và lọc chất lỏng nổi bên trên qua một phễu lọc
thô và cho thêm vật liệu cấy này vào các bình thử để đạt được nồng độ trong môi trường thử từ 1 %
(V/V) đến 5 % (V/V). Nếu cần có thể sử dụng lượng vật liệu cấy nhiều hơn nhưng
điều này có thể dẫn đến những vấn đề trong việc hình thành cân bằng cacbon. Việc
sử dụng compost có thể làm gia tăng số
lượng nấm có trong bình
thử và cải thiện quá trình phân hủy sinh học của vật liệu chất dẻo. Trong trường
hợp này cần phải nêu rõ trạng thái compost được sử dụng trong báo cáo thử nghiệm
(ví dụ compost đã ngấu,
compost lấy từ pha nóng ở khoảng 50 °C).
Khi cần phải có nồng độ vật
liệu cấy cao hơn thì hòa lượng đất
hoặc compost nhiều hơn vào
trong
môi trường thử và pha loãng đến nồng độ thích hợp cho quá trình ủ.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Chuẩn bị một số lượng các bình thử sao
cho phép thử ít nhất phải có:
a) Hai bình thử dùng để chứa
vật liệu thử (ký hiệu FT);
b) Hai bình thử dùng để chứa mẫu
trắng (ký hiệu FB);
c) Một bình thử dùng để kiểm tra hoạt
tính của vật liệu
cấy sử dụng vật liệu đối
chứng
(ký hiệu FC).
Và nếu có yêu cầu:
d) Một bình thử dùng để kiểm tra khả
năng phân hủy không sinh học hoặc sự thay đổi không sinh học trong vật liệu thử,
ví dụ bằng
phương pháp thủy phân (ký hiệu Fs). Dung dịch thử ở
trong bình Fs
phải được tiệt trùng, ví dụ như hấp bằng
nồi hấp hoặc bổ sung thêm hợp chất vô cơ thích hợp để ngăn chặn hoạt tính của vi sinh vật. Ví dụ sử dụng 5
ml/l dung dịch có chứa 10 g/l
thủy ngân (II) clorua (HgCI2). Nếu có yêu cầu thì trong quá
trình thử có thể bổ sung thêm
cùng một lượng tương tự chất độc này.
e) Một bình dùng làm đối chứng
âm (ký hiệu FN), sử dụng một
polyme không phân hủy sinh học (ví
dụ polyetylen) có cùng kích thước và hình dạng với vật liệu thử.
f) Một bình dùng để kiểm tra tác động ức chế của vật
liệu thử đến hoạt động của vi sinh vật (ký hiệu Fl). Đảm bảo rằng
tỷ lệ giữa cacbon trong vật liệu thử và vật liệu đối chứng với
nitơ trong môi trường ít nhất là C:N - 40:1. Bổ sung thêm nitơ nếu có yêu cầu.
Cho đủ môi trường thử
(6.2) và vật liệu cấy (8.3) vào các bình thử theo như quy định tại Bảng 1.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Bình thử
Vật liệu thử
Vật liệu đối chứng
Vật liệu cấy
FT Mẫu thử
+
-
+
FT Mẫu thử
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
-
+
FB Mẫu trắng
-
-
+
FB Mẫu trắng
-
-
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
FC Kiểm
tra vật liệu cấy
-
+
+
Fs Kiểm tra sự phân hủy không sinh học (tùy
chọn)
+
-
-
Fl Kiểm tra ức
chế (tùy chọn)
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
+
+
Fs Kiểm tra âm tính (tùy chọn)
-
+
+
Nối các bình thử vào hệ thống tạo
không khí không chứa CO2 (xem Phụ lục
A). Ủ tại nhiệt độ
thử mong muốn (xem Điều 5) và sục khí các bình trong 24 h để đuổi hết cacbon dioxit ra khỏi
hệ thống. Nếu thực hiện ở nhiệt độ cao
hơn thì phải ngăn chặn
việc bổ sung hoặc mất mát chất lỏng bằng thiết bị phù hợp. Sử dụng máy
lắc hoặc máy khuấy để khuấy trộn hỗn hợp
thử. Nếu quan sát thấy hiện tượng tạo bọt quá nhiều thì thay việc thổi khí bằng
việc sục khí ở phía trên, có khuấy
trộn. Sau khi sục khí sơ bộ thì nối đầu không
khí ra của từng
bình vào hệ thống
bẫy hoặc đo cacbon dioxit.
Nếu xác định cân bằng cacbon (xem Phụ
lục C) thì lấy một lượng
thể tích biết trước
vừa đủ của môi trường thử đã cấy từ mỗi bình hoặc từ
các bình tách biệt
để xác định DOC và sinh khối tại thời điểm bắt đầu và kết thúc của quá trình ủ.
Khi điều chỉnh thể tích cuối cùng hoặc khi tính toán kết quả thử phải lưu ý đến
lượng thể tích đã lấy ra này.
Cho vật liệu thử (8.1), vật liệu đối
chứng và vật liệu kiểm chứng âm
tính (8.2) vào các bình tương ứng
như nêu trong Bảng 1 và bắt đầu phép thử bằng cách thổi sục không khí không chứa
CO2 vào các bình để cung cấp đủ lượng oxy cần
cho phép thử. Tốc độ thổi từ 50 ml/min
đến 100 ml/min là thích hợp.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Khi lượng cacbon dioxit giải phóng ra đạt
giá trị ổn định (đạt đến giai đoạn ổn định) và không có thêm sự phân hủy sinh học
xảy ra thì phép thử coi
như đã hoàn thành. Thời gian tối đa là 6 tháng. Trong trường hợp thời
gian thử
dài thì phải lưu ý đặc biệt
đến hệ thống thiết bị (ví dụ độ kín khít của bình thử và hệ thống kết nối, đảm
bảo không có cacbon dioxit từ bên ngoài đi vào và không bị rò rỉ).
Tại thời điểm kết thúc phép thử, đo
pH, axit hóa tất cả các chai bằng 1 ml axit clohydric đậm đặc để phân hủy cacbonat hoặc bicacbonat và
thổi khí để đuổi cacbon
dioxit. Tiếp tục sục khí trong 24 h
và đo lượng cacbon dioxit sinh ra trong mỗi bình của dãy các bình (FT, FB, FC...).
9 Tính toán và biểu
thị kết quả
9.1 Tính toán
9.1.1 Lượng cacbon
dioxit sinh ra bởi vật liệu thử
Tính lượng cacbon dioxit sinh ra theo
lý thuyết (ThCO2) theo công
thức (1), biểu thị bằng miligam:
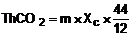 (1)
(1)
Trong đó
m là khối lượng của vật
liệu thử cho vào trong bình thử, tính
bằng miligam;
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
44 và 12 là khối lượng
phân tử của cacbon
dioxit
và khối lượng nguyên tử
của
cacbon.
Tính toán lượng cacbon dioxit sinh ra
theo lý thuyết từ vật liệu đối chứng và hỗn hợp của vật liệu thử và vật liệu đối
chứng trong bình
Fl.
9.1.2 Phần trăm
phân hủy sinh học từ lượng
CO2 sinh ra
Từ lượng cacbon dioxit trong mỗi
phép đo, tính phần trăm phân hủy sinh học Dt của mỗi bình thử FT theo phương trình (2):
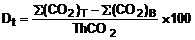 (2)
(2)
Trong đó
∑(CO2)T là lượng cacbon
dioxit sinh ra trong từng bình thử FT từ khi bắt đầu phép thử cho đến thời gian t,
tính bằng miligam;
∑(CO2)B là lượng
cacbon dioxit sinh ra
trong bình chứa mẫu trắng FB từ khi bắt đầu phép
thử đến thời gian t, tính bằng mlligam
ThCO2 là lượng
cacbon dioxit sinh ra theo lý thuyết từ vật liệu thử, tính bằng
miligam.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Nếu tính cân bằng cacbon thì tính mức độ
phân hủy sinh học của vật liệu thử từ lượng cacbon dioxit sinh ra
và hàm lượng
cacbon trong sinh khối sinh ra
trong quá trình thử (Phụ lục C).
9.2 Biểu thị và
giải thích kết quả
Lập bảng các giá trị cacbon dioxit
sinh ra và giá trị phần trăm phân hủy sinh học tương ứng với từng thời điểm đo và của mỗi
bình thử. Đối với mỗi bình thử, vẽ đồ
thị đường cong của
lượng cacbon dioxit sinh ra và đường cong phần trăm phân hủy sinh học theo thời
gian. Nếu thu được các kết quả có thể so sánh đối với hai bình thử tiến
hành đồng thời thì có thể vẽ đường
cong trung bình.
Mức phân hủy sinh học tối đa được xác
định là giá trị trung bình của giai
đoạn ổn định trên đồ thị
phân hủy sinh học hoặc giá trị cao nhất, ví dụ khi đồ thị đi xuống hoặc đi lên chậm trong giai đoạn ổn định, mô tả
mức độ phân hủy sinh học của vật liệu thử. Nếu cân bằng cacbon đã được xác định thì kết quả của
xác định này mô tả
tổng mức độ
phân hủy sinh học.
Khả năng thấm ướt và hình dạng của
các miếng vật liệu thử có thể ảnh hưởng đến kết quả và phải tính đến điều
này khi so sánh các
kết quả thu được từ các vật liệu chất dẻo có cấu trúc hóa học giống nhau.
Thông tin về độc tính của vật liệu thử
có thể sẽ hữu ích
trong việc giải thích các kết quả thử chỉ ra
khả năng phân hủy sinh học thấp.
10 Độ tin cậy của kết
quả
Phép thử được coi là tin cậy nếu
a) Mức độ phân hủy sinh học của vật liệu
đối chứng (bình kiểm tra vật liệu
cấy FC) lớn hơn 60
% tại thời điểm kết thúc phép thử;
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Nếu trong bình Fl (kiểm tra ức chế,
nếu có) phần trăm phân hủy sinh học < 25 % và không quan sát được rõ
sự phân hủy của vật liệu thử thì có thể coi như vật liệu thử gây ức chế.
Nếu trong bình Fs
(kiểm tra phân hủy
không sinh học, nếu có) quan sát được rõ lượng
cacbon dioxit (> 10 %) thì quá trình phân hủy không sinh học có thể đã xảy ra.
Nếu có bình FN
(kiểm tra âm tính) thì
sẽ
không quan sát có cacbon
dioxit sinh ra.
Nếu các tiêu chí này không đạt
được thì lặp lại phép thử bằng cách sử
dụng lượng vật liệu cấy được làm
thích nghi trước hoặc được tiếp xúc trước.
11 Báo cáo thử nghiệm
Báo cáo thử nghiệm phải bao gồm ít nhất các thông
tin sau đây:
a) viện dẫn tiêu chuẩn này;
b) tất cả thông tin cần thiết để nhận biết vật
liệu thử và vật liệu đối chứng, gồm TOC, ThCO2, thành phần và công
thức hóa học (nếu biết), hình dạng, thể loại và hàm lượng/nồng độ trong các mẫu thử;
c) các thông số thử chính, gồm thể tích thử,
môi trường thử sử dụng, nhiệt
độ ủ và pH cuối;
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
e) kỹ thuật phân tích được sử dụng gồm
nguyên tắc của hô hấp
kế và phương pháp xác định TOC, DOC và sinh khối;
f) tất cả các kết quả thử thu được đối
với vật liệu thử
và vật liệu đối chứng (dạng bảng biểu và đồ thị) bao gồm lượng cacbon dioxit cộng dồn
đo được, các giá trị phần trăm phân hủy sinh học và đồ thị tương ứng của các
thông số này theo thời gian;
g) khoảng thời gian của giai đoạn
thích ứng và giai đoạn phân hủy sinh học, mức phân hủy sinh học tối đa cũng như
tổng thời gian thử;
và các thông tin tùy chọn sau, nếu có
thực hiện hoặc xác định:
h) kết quả quá
trình kiểm tra sự phân hủy không sinh học Fs, kiểm tra ức chế FT và kiểm tra
âm tính
FN;
i) kết quả việc xác định cân bằng
cacbon, bao gồm như:
1) lượng cacbon trong vật liệu thử bị
oxy hóa thành cacbon dioxit,
2) lượng tăng DOC trong môi trường thử
trong quá trình ủ gây ra bởi các chất có thể hòa tan trong nước,
3) lượng tăng cacbon hữu cơ trong sinh
khối trong quá trình thử,
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
5) tổng số lượng cacbon đo
được, biểu thị bằng phần trăm cacbon được đưa vào thông qua vật liệu thử;
j) đơn vị cụm khuẩn (cfu/g) có trong hỗn
hợp thử được cấy;
k) bất kỳ dữ liệu nào có liên quan (ví
dụ khối lượng phân tử ban đầu của mẫu thử, khối lượng phân tử của polyme tồn
dư);
Phụ
lục A
(tham
khảo)
Nguyên tắc của hệ thống do lượng cacbon
dioxit sinh ra (ví dụ)
Các bình được lắp theo dãy
như nêu trong Hình A.1 và được
nối với nhau bằng
các ống không thấm
khí. Dẫn không khí không chứa CO2 với tốc độ từ
50 ml/min đến 100 ml/min vào trong hệ
thống ở áp suất thấp không đổi. Kiểm tra tốc độ dòng khí bằng cách đếm
bọt khí hoặc sử dụng
thiết bị kiểm soát tốc độ
dòng phù hợp. Sử dụng khi tổng
hợp không chứa CO2 hoặc khí
nén. Trong trường hợp sử dụng khí nén thì loại bỏ khí CO2 bằng cách cho khí đi
qua một chai (3) chứa natri cacbonat khô hoặc cho qua ít nhất hai bình rửa khí
có chứa, ví dụ như 500 ml dung dịch kali hydroxit 10 mol/L. Có thể sử dụng thêm
một bình có chứa
100 ml dung dịch bari hydroxit 0,0125 moI/L và một bình rỗng để nhận
biết sự hiện diện của CO2 trong khí
khi nó
làm
đục dung dịch này và để ngăn việc cuốn theo chất lỏng vào trong bình thử nghiệm. Có
thể sử dụng một bình rỗng, ở giữa
bình thử và bình chứa chất,
chỉ thị để ngăn chặn sự
kéo theo chất lỏng. CO2 sẽ được sinh
ra trong các bình thử nếu quá trình phân hủy
sinh học xảy ra và được hấp thụ trong một chai tiếp theo có chứa chất hấp thụ để
xác định như mô tả trong Phụ lục B.

...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
1
Không khí nén
5
Bình thử
2
Kiểm soát tốc độ dòng
6
Thiết bị khuấy
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Bẫy cacbon dioxit (ví dụ hai chai rửa có
chứa
kiềm)
7
Bẫy cacbon dioxit (ví dụ hai chai rửa có chứa kiềm)
4
Chất chỉ thị cacbon
dioxit [Ba(OH)2]
Hình A.1
Phụ
lục B
(tham
khảo)
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
B.1 Xác định CO2 bằng cách đo
DIC
Khí cacbon dioxit sinh ra được hấp thụ
trong dung dịch natri hydroxit (NaOH) và được xác định là cacbon vô cơ
hòa tan (DIC) bằng máy phân tích DOC mà không cần tro hóa.
Chuẩn bị dung dịch 0,05 mol/L NaOH trong nước khử ion. Đo
lượng DIC của dung dịch này và sử
dụng giá trị mẫu trắng này khi tính CO2 sinh ra. Nối vào dây
bình thử nghiệm
hai chai chứa chất hấp thụ, mỗi
chai chứa 100 ml dung dịch NaOH. Dùng một xi phông nhỏ đóng đầu ra của chai cuối cùng để
ngăn CO2 từ không khí bên ngoài đi
vào dung dịch NaOH. Vào các ngày xác định CO2, lấy chai chứa chất hấp thụ sát cạnh bình thử nghiệm
và lấy lượng,
mẫu
thử đủ lớn để đo DIC (ví dụ
10 ml). Thay chai này bằng chai thứ hai và thêm một chai mới chứa dung dịch
NaOH chưa sử dụng vào. Vào ngày cuối cùng, sau khi axit hóa dung dịch
thử, đo lượng DIC trong cả hai chai.
Tính lượng CO2 sinh ra theo
phương trình (C.1)
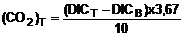 (C.1)
(C.1)
Trong đó
(CO2)T là lượng CO2 sinh
ra, tính bằng miligam;
DICT là lượng
DIC đo được, tính bằng
miligam
DlCB là lượng
DIC đo được trong bình trắng đối với dung dịch NaOH, tính bằng millgam;
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
10 là hệ số hiệu chỉnh cho việc sử dụng 100 ml
dung dịch NaOH.
B.2 Phương pháp
chuẩn độ bằng dung dịch bari hydroxyt
Lượng CO2 sinh ra phản
ứng với bari hydroxyt [Ba(OH)2] và kết tủa thành bari cacbonat (BaCO3) [xem phản ứng (C.2)]. Lượng
cacbon dioxit sinh ra được xác định bằng phương pháp chuẩn độ dung dịch Ba(OH)2
dư với axit clohydric (HCl) [xem phản ứng (C.3)].
CO2 + Ba(OH)2
→ BaCO3 + H2O (C.2)
Ba(OH)2 + 2 HCl → BaCI2
+ 2H2O (C.3).
Hòa tan 4,0 g Ba(OH)2.8H2O
vào nước khử ion hoặc nước cất tạo thành 1 000 ml để thu được dung dịch 0,0125
mol/L. Nên chuẩn bị
một
lượng đủ vào, thời điểm thực hiện
chuỗi phép thử, ví
dụ khoảng 5 L.
Lọc vật liệu rắn và xác định chính xác nồng độ bằng phương pháp chuẩn độ với dung
dịch HCl chuẩn.
Dùng phenolphtalein làm chất chỉ thị hoặc một máy chuẩn độ tự động để xác định điểm kết thúc. Giữ dung dịch sạch
trong một bình thử được niêm
phong nhằm ngăn sự hấp thụ CO2 từ không khí.
Pha loãng 50 ml dung dịch HCl 1 mol/l (36,5 g/l) đến
1 000 ml với nước khử ion hoặc nước cất để thu được dung dịch 0,05 mol/L.
Khi bắt đầu phép thử, cho chính xác
100 ml dung dịch Ba(OH)2
vào từng chai trong ba chai chứa chất hấp thụ. Tùy vào đặc điểm và lượng vật
liệu thử mà điều chỉnh thể tích dùng để bẫy. Định kỳ lấy chai sát với bình thử nghiệm
để chuẩn độ. Cũng có thể chuẩn độ khi cần
thiết ví
dụ
như khi chai thứ nhất
bị vẩn đục hay trước khi quan
sát được kết tủa BaCO3 trong chai
thứ hai. Khi bắt đầu phép thử cần chuẩn độ cách ngày và khi đạt đến giai đoạn ổn định thì
cách năm ngày chuẩn độ một lần.
Sau khi lấy chai hấp thụ ra,
ngay lập tức đậy
lại để ngăn CO2 từ không khí
đi vào. Chuyển vị trí hai chai còn
lại vào vị trí gần với bình thử nghiệm
và đặt vào cuối dãy một chai mới chứa dung dịch Ba(OH)2 mới. Đặc biệt nếu
phép thử diễn ra lâu hơn, xác định chính xác nồng độ của dung dịch. Xử
lý tương tự với tất cả các bình chứa vật liệu thử, vật liệu đối chứng, mẫu trắng,
bình kiểm soát ức chế và
bình kiểm soát
vật liệu cấy.
Ngay khi tháo chai ra,
chuẩn độ hai hoặc
ba phần của dung dịch Ba(OH)2 bằng dung dịch HCl. Ghi lại thể tích
dung dịch HCl cần để trung hòa.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
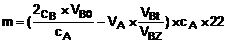 (C.4)
(C.4)
Trong đó:
m là khối lượng CO2 bị bẫy trong
chai hấp thụ, tính bằng miligam;
cA là nồng độ chính xác của
dung dịch HCl, tính
bằng mol
trên
lít;
cB là nồng độ
chính xác của
dung dịch Ba(OH)2, tính bằng mol trên lít;
VB0 là thể tích của
dung dịch Ba(OH)2 khi bắt đầu phép thử, tính bằng
mililit;
VBt là thể tích của
dung dịch Ba(OH)2
vào thời điểm t trước khi chuẩn độ, tính bằng mililit;
VBz là thể tích của
phần dung dịch Ba(OH)2 dùng để chuẩn độ, tính bằng
mililit;
VA là thể tích dung dịch
HCl dùng để chuẩn độ, tính bằng mililit;
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Khi áp dụng các điều kiện sau:
- thể tích của dung dịch Ba(OH)2 trước
và sau khi hấp thụ chính xác là 100
ml;
- toàn bộ dung dịch dùng để chuẩn độ (VB0 = VBt=VBz);
- nồng độ CB của dung dịch Ba(OH)2
chính xác là
0,0125 mol/l;
- nồng độ CA của dung dịch HCl chính
xác là 0,05 mol/l;
sử dụng phương trình (C.5)
m = 1,1 x (50 - VA) (C.5)
Phụ
lục C
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Ví dụ về việc xác định cân bằng cacbon
C.1 Nguyên tắc
Vật liệu chất dẻo thường có thành phần
phức tạp hơn so
với
các hợp chất phân tử
thấp. Việc xác định riêng sự giải phóng CO2 hoặc BOD thường là
không đủ để xác định đặc tính và chất lượng của khả năng phân hủy sinh học. Trong quá
trình phân hủy sinh học, sinh khối mới
được hình thành bởi các vi sinh vật và một phần của
cacbon có trong vật liệu thử được chuyển vào sinh khối nhưng không bị oxy hóa sinh
học. Do vậy, các thông số phân tích như sự giải phóng CO2 và BOD thường không
đạt được đến 100 % giá trị lý thuyết
mong muốn, mặc dù trong trường hợp này sự phân hủy sinh học của vật liệu
thử là hoàn toàn và
sự phân rã không đủ có thể bị suy luận không đúng từ các kết quả thử. Việc xác định
cân bằng cacbon như mô tả trong phụ lục
này có thể hữu ích trong các
trường hợp xác nhận lại khả năng phân hủy sinh học hoàn toàn. Vì một cân bằng
dựa trên tổng lượng cacbon thu được từ các phép đo sau: lượng cacbon có trong cacbon
dioxit, lượng cacbon được sinh ra dưới dạng sinh khối mới, lượng cacbon chuyển
vào các chất chuyển hóa hữu cơ tan trong
nước, lượng cacbon xác định dưới dạng
DOC và lượng cacbon còn lại trong vật liệu polyme chưa được phân hủy. Tổng cacbon được
so sánh
với
lượng cacbon hữu cơ trong vật liệu thử được đưa vào trong hệ thống thử.
C.2 Cách tiến hành
Xác định BOD sinh ra như mô tả trong
8.4.
Lấy các mẫu của môi trường đã cấy tại thời điểm bắt đầu,
trước khi cho thêm vật liệu thử và tại thời điểm kết thúc quá trình ủ. Việc lấy mẫu
phải được tiến hành cẩn thận để thu
được các mẫu thử
đại
diện. Cho các mẫu qua một tấm lọc màng hoặc ly tâm chúng ở tốc độ khoảng 40 000 m.s-2.
Với từng mẫu, xác định lượng sinh khối
trong chất lọc ra hoặc ly tâm theo phương pháp phù hợp, ví dụ bằng phép đo
protein. Xác định hoặc tính lượng
cacbon trong sinh khối và tính toán sự chênh lệch này từ lượng tăng của cacbon
hữu cơ trong sinh khối.
Xác định theo ISO 8245, DOC trong chất
lọc của từng mẫu và
tính toán lượng
tăng cacbon hữu cơ. Nếu có thể, nhận dạng hợp chất hình thành DOC để xác nhận lại sự hình thành của
các chất chuyển hóa
tan trong nước.
Sử dụng toàn bộ mỗi lượng mẫu còn lại
để xác định lượng cacbon trong polyme cặn tại thời điểm kết thúc
phép thử. Đây thường là
quy trình khó khăn và có
thể làm hoặc trực tiếp có thể phân tích riêng polyme (xem phụ lục F) hoặc
gián tiếp. Trong
trường
hợp trực tiếp, chiết và cân polyme cặn và tính lượng cacbon từ thành phần
đã biết của
polyme. Một phương pháp xác định gián tiếp là rửa, sấy khô, cân phần cặn và xác
định cacbon hữu cơ tổng (TOC). Sau đó trừ đi giá trị cacbon sinh khối (nêu trên) để thu được lượng
cacbon có trong polyme
cặn. Một cách khác là cân chính xác cặn và xử lý chúng bằng phương pháp thích hợp
để phá hủy sinh khối nhưng không phá hủy các polyme (điều này phải được kiểm
tra trước). Ví dụ như sử dụng natri hypoclorit, loại bỏ phần hòa tan và cân lại
mẫu. Coi như tất cả sinh khối đã bị loại bỏ và tính toán từ
khối lượng thu
được hàm lượng cặn polyme.
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Tính lượng cacbon bị oxy hóa sinh
học CBOD (mg/l) trong
vật liệu thử được đưa vào trong hệ thống thử (hàm lượng cacbon CMAT) từ phần
trăm phân hủy sinh học Dt thu được trong phép thử hô hấp kế
(xem 9.1), theo công thức C.1:
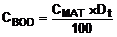 (C.1)
(C.1)
Tính toán lượng tăng của cacbon sinh khối
trong các bình thử có chứa vật liệu thử CBlO (mg/I) bằng
cách so sánh sinh khối tại thời điểm bắt đầu với thời điểm kết thúc quá trình ủ,
lưu ý đến lượng cacbon có trong sinh khối đo được hoặc ước lượng được CB (bắt đầu) và CB(kết thúc) theo công thức C.2.
CBIO= CB (bắt đầu) - CB
(kết thúc) (C.2)
Xác định lượng tăng DOC trong suốt quá trình ủ CDOC (mg/l) bằng
cách so sánh nồng độ DOC tại thời điểm bắt đầu với thời điểm kết thúc theo công
thức (C.3)
CDOC=DOC(kết thúc) - DOC (bắt đầu) (C.3)
Xác định lượng cacbon hữu cơ trong các
polyme cặn tại thời
điểm kết thúc phép thử CPOL
Tính giá trị chênh lệch của các lượng cacbon chuyển
hóa theo phần trăm của cacbon đưa vào CMAT và cộng lại
để thu được cacbon tính toán CCALC (%) theo công thức
C.4:
CCALC = CBOD + CBIO + CDOC + CPOL (C.4)
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Cho vật liệu thử: CMAT = 600 mg/l =
334,8 mg/l cacbon
Mức độ phân hủy sinh học: Dt = 78 %
CB(bắt đầu)
CB(kết thúc)
CBIO
DOC(bắt đầu)
DOC(kết thúc)
DOC
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
mg/l
3,2
61,0
57,8
2,0
22,0
20,0
261
% CMAT
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
17,2
6,0
78
Tính cân bằng cacbon: CCALC = 78 %
+ 17 % + 6 % = 101 % CMAT
Phụ
lục D
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
Ví dụ xác định lượng và khối lượng phân tử của
polyme không hòa tan trong nước còn lại khi kết thúc phép thử phân hủy sinh học
Sử dụng quy trình đo lượng
và khối lượng phân tử của các
polyme còn lại khi kết thúc
nghiên cứu có thể hữu dụng. Có thể dùng phương pháp sau đây hoặc phương pháp
thích hợp khác để phân tích các polyme không hòa tan trong nước nhưng
hòa tan trong dung môi
hữu
cơ không trộn được với nước.
a) Cho hỗn hợp kiểm tra vào phễu
chiết, thêm dung môi hữu cơ thích hợp và lắc trong 10 min đến 20 min để chiết
các polyme còn lại. Tách lớp dung môi hữu cơ ra khỏi lớp dung dịch. Thêm dung
môi mới và lặp lại
quy trình.
b) Trộn lẫn các phần hữu cơ chiết được ra và
cho bay hơi dung môi đến khô. Hòa tan mẫu chất rắn trong một
thể tích nước giải hấp thích hợp.
c) Sử dụng một bơm tiêm vi lượng, tiêm
một lượng thích hợp vào thiết bị sắc ký lỏng hiệu năng cao (HPLC) có một cột chứa
gel sử dụng trong sắc ký khí thẩm thấu gel. Bắt đầu phân tích và ghi phổ.
d) Xác định lượng polyme có mặt bằng
cách sử dụng đồ thị hiệu chuẩn.
e) Xác định khối lượng phân tử polyme
bằng cách tiêm vào trong sắc phổ polyme cùng loại, hoặc polyme có cấu trúc
tương tự polyme thử mà đã
biết khối lượng phân tử. Mối liên hệ giữa thời gian lưu và khối lượng phân
tử thu được từ
sắc phổ cuối cùng. Tính khối lượng phân tử từ liên hệ này.
Khối lượng phân tử của polyme thử cũng
có thể xác định được bằng phương pháp HPLC với detector loại kết hợp giữa quét
tia-laser góc hẹp (LALLS) và chỉ số khúc xạ vi sai (RI).
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
(tham
khảo)
Thư mục tài liệu tham khảo
[1] ASTM D 3536-91, Molecular
weight averages and molecular weight distribution by liquid exclusion
chromatography (GEL permeation chromatography- GPC).
[2] ISO 8192:1986, Water quality
- Test for inhibition of oxygen consumption by activated sludge.
[3] ISO 11923, Water quality -
Determination of suspended solids by filtration through glass-fibre filters.
[4] MüLLER, R.-J., AUGUSTA,
J., and PANTKE, M. (1992), An Interlaboratory Investigation Into Biodegradation
of Plastics; Part 1: A Modified Sturm Test, Material and Organisms, 27/3,
pip. 179- 189.
[5] PüCHNER, p., MUELLER,
W.R., and BARDTKE, D. (1995), Assessing the Biodegradation Potential of
Polymers in Sreening and Long-term Test Systems, J.Environm. Polymer
Degradation, 3, pp. 133-143.
[6] PüCHNER, P., MUELLER,
W.R., and BARDTKE, D. (1995), Assessing the ӓaeroben und anaeroben bedingungen,
Dissertation, Stuttgart University Fakultat für Bauingenieurwesen,
Stuttgarter Berichte zur Abfallwirtschaft, 59, Erich Schmidt
Verlag, Berlin.
[7] SPERANDIO, A., and PüCHNER, P. (1993),
Bestimmung der Gesamtprotelne als Biomasse- Parameter in wӓßrigen Kulturen und
auf Trӓgermaterialien aus Bio-Reaktoren, gwf Wasser; Abwasser, 134,
pp.482-485,
...
...
...
Bạn phải
đăng nhập hoặc
đăng ký Thành Viên
TVPL Pro để sử dụng được đầy đủ các tiện ích gia tăng liên quan đến nội dung TCVN.
Mọi chi tiết xin liên hệ:
ĐT: (028) 3930 3279 DĐ: 0906 22 99 66
2) Thu
thập từ: Puchner (1994) (tài liệu tham khảo [6] trong phụ lục E)
